|
|
|---|
Pada tahun 1919, Niel Bohr telah mengemukan model atomnya. Bagi menghuraikan teori tersebut , model atom hidrogennya diandaikan mempunyai ciri-ciri berikut :
1. Elektron bergerak dalam petala di sekitar nukleus tetapi hanya petala tertentu dibenarkan
2. Elektron hanya boleh duduk pada aras
tenaga yang tenaga tertentu sahaja (disktret). Lebih jauh
dari nukleus lebih tinggi aras tenaga petala itu.
Jika ![]() mewakili
1 proton,
mewakili
1 proton, ![]() 1 neutron dan
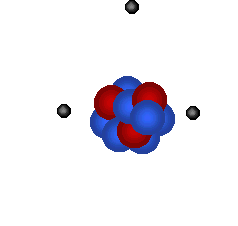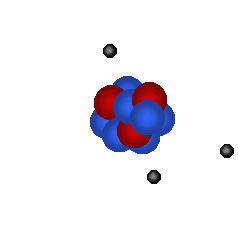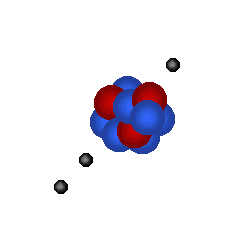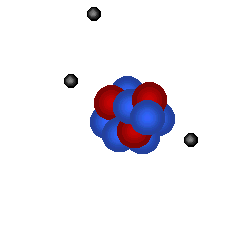
1 neutron dan ![]() satu elektron model, satu atom hidrogen, helium dan litium dapat diwakilkan
oleh simulasi berikut:
satu elektron model, satu atom hidrogen, helium dan litium dapat diwakilkan
oleh simulasi berikut:
 |
 |
 |
|
Kofigurasi elektron: |
Konfigurasi elektron: |
Konfigurasi elektron : |
Perlu diingatkan satu atom hidrogen adalah tersangat kecil iaitu berjejari 5 x 10 -7 mm Titik sebesar 1 mm boleh dipenuhi oleh 20 juta atom hidrogen! Jarak sebenar antara nukleus dan elektron adalah tersangat besar dibandingkan dengan jejari nukleus. Jika proton hidrogen tersebut diwakili sebuah bola sepak, jika bole sepak ini diletakkan ditengah padang di Bukit Jalil, elektronnya akan berputar di sekitar tangga-tanga tempat duduk penuntun. Olehitu adalah mustahil untuk melukis model atom dalam nisbah sebenarnya di atas sekeping kertas!
Seperkara lagi yang perlu diingat ialah
jisim
relatif elektron adalah tersangat jauh lebih kecil dibandingkan
degan sebiji proton . Jika proton dikatakan mempunyai sifat jirim
elektron pula dikatakan menunjukkan sebahagian ciri-ciri gelombang.
Simulasi dibawah cuba sebanyak sedikit dapat menggambarkan keadaan ini.
 |